Pandèmia
La FDA als EUA endureix els requisits per a la vacuna contra la Covid-19
L'Administració d'Aliments i Medicaments va publicar noves regulacions, entre les quals destaca fer un seguiment d'almenys dos mesos en els voluntaris després de rebre la dosi final
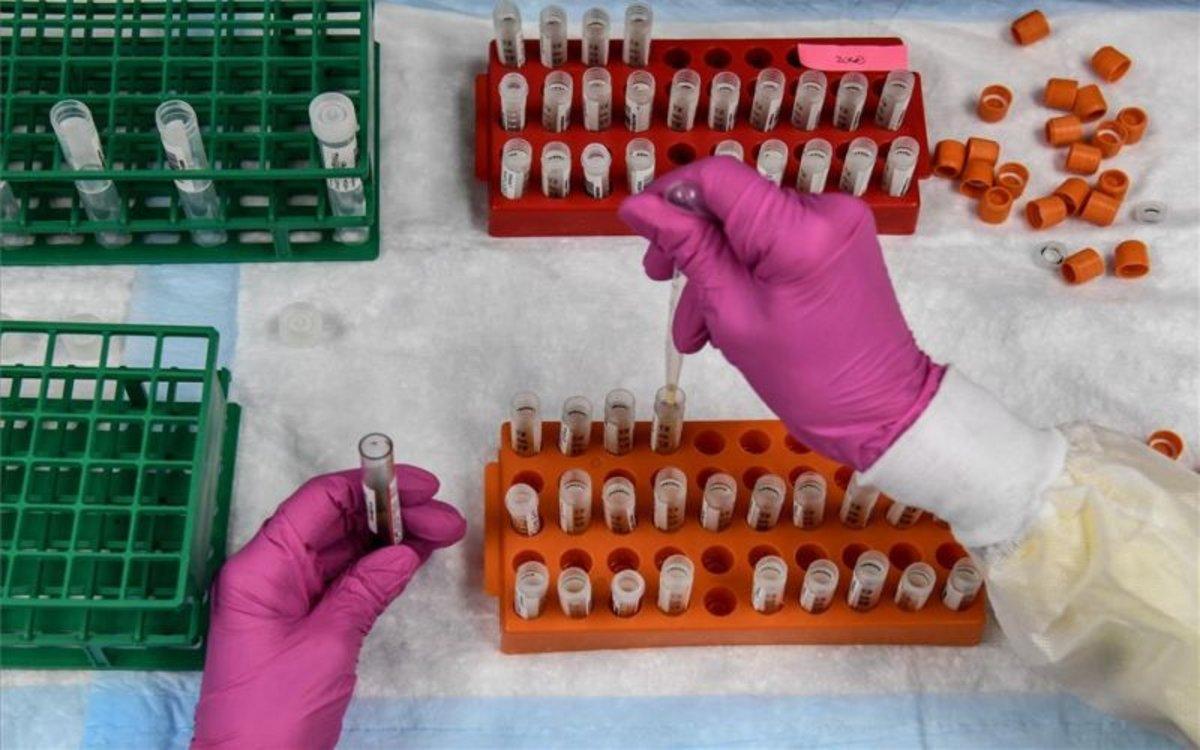
coronavirus-vacuna-eeuu
L’Administració d’Aliments i Medicaments dels EUA (FDA, en anglès) va publicar aquest dimarts una guia amb nous requisits per a l’aprovació d’una futura vacuna contra la Covid-19, entre els quals, fer un seguiment durant almenys dos mesos als voluntaris després d’aplicar-los la dosi final durant la fase de prova, cosa que podria retardar la sortida al mercat de les actuals candidates.
«Les dades dels estudis de fase 3 han d’incloure una durada mitjana de seguiment d’almenys dos mesos després de finalitzar el règim complet de vacunació per ajudar a proporcionar informació adequada per avaluar el perfil de beneficis i riscos de la vacuna», va assenyalar la FDA a la guia.
A més, l’agència governamental va requerir que els fabricants documentin cinc casos d’infecció greu en persones que van rebre el placebo en comptes de la vacuna provada.
Retarden els plans de Trump
Les noves directrius podrien retardar la sortida de la futura vacuna, cosa que xocaria amb els plans del president nord-americà i candidat republicà a la reelecció, Donald Trump, que va arribar a suggerir que podria estar disponible fins i tot abans de les eleccions del pròxim 3 de novembre, en què es juga la seva continuïtat en el càrrec.
Mitjans locals van assenyalar, no obstant, que la FDA va publicar unilateralment els nous estàndards en el seu lloc web, que van ser finalment aprovats per la Casa Blanca.
El diari The New York Times va indicar que funcionaris de la Casa Blanca van bloquejar «durant dues setmanes» les noves pautes, i va assenyalar que el «canvi abrupte» es va adoptar després que aquest diari publiqués que treballadors del Govern, inclòs el cap del gabinet, Mark Meadows, retenien la nova reglamentació.
Avenç de les vacunes
Una de les objeccions dels funcionaris de la Casa Blanca era que les directrius afegien més temps al període d’aprovació de la possible vacuna, segons el diari novaiorquès.
Notícies relacionadesQuatre possibles vacunes es troben en l’etapa final de prova, anomenada assaig de fase 3 als Estats Units, mentre que un cinquè estudi s’espera que comenci aquest mes, va puntualitzar el ‘Times’.
Sobre això, la presidenta de la Cambra de Representants, la demòcrata Nancy Pelosi, va advertir en un comunicat que l’anomenada ‘autorització d’ús d’emergència’ per a qualsevol vacuna contra el coronavirus, és a dir, sense aprovació, «ha de ser determinada per estàndards clars per garantir seguretat i eficiència».
- Les principals cases d’apostes ja tenen un candidat favorit per ser el nou Papa
- Els bojos són ells, ells
- Final de la Copa del Rei Les 8 hores que van portar el futbol espanyol al caire de l’abisme: «El Madrid no ens pot demanar que canviem els àrbitres»
- Kounde decideix una final apoteòsica
- Flick despulla el Madrid (cap. III)
- La caixa de ressonància ¿Un concert pot competir amb un Barça-Madrid?
- Loteries Números premiats a la Grossa de Sant Jordi 2025: primer, segon i tercer premi
- Mil anys d’aniversari Montserrat rep amb devoció la sortida de la Moreneta per primera vegada en aquest mil·lenni
- Gairebé dos milions de persones La retransmissió de la Copa del Rei a TV3, l’emissió en directe més vista de la temporada
- Creu de Sant Jordi 2019 Mor Montserrat Úbeda, referent de la catalanitat i ànima d’Ona Llibres

